Luego de revisar los resultados de las más recientes pruebas clínicas, la FDA ha concluido que es "poco probable" que esta medicina produzca un efecto "antiviral".
Ciudad de México, 15 de junio (RT).- La Administración de Alimentos y Medicamentos de EU (FDA, por sus siglas en inglés) anunció este lunes que ha revocado su autorización de uso de emergencia de cloroquina e hidroxicloroquina, fármacos desarrollados originalmente contra la malaria, para combatir la COVID-19.
La jefa científica de la FDA, Denise Hinton, comunicó que tras revisar la nueva información de los recientes ensayos clínicos, el organismo llegó a la conclusión de que "es poco probable" que los regímenes de dosificación sugeridos "produzcan un efecto antiviral".
"Además, a la luz de los graves casos cardíacos en curso y otros efectos secundarios graves, los beneficios conocidos y potenciales de la cloroquina y la hidroxicloroquina ya no superan los riesgos conocidos y potenciales para el uso autorizado", afirmó la agencia.
Ambas medicinas, de varias décadas de antigüedad, también recetadas para combatir el lupus y la artritis reumatoide, pueden causar problemas en el ritmo cardíaco, reducir severamente la presión arterial y provocar daño muscular o nervioso.
El anuncio significa que los envíos de esos medicamentos obtenidos por el gobierno federal ya no se distribuirán a las autoridades de salud estatales y locales. Los medicamentos, sin embargo, aún estarán disponibles para usos alternativos, por lo que los médicos estadounidenses aún podrían recetarlos para COVID-19, una práctica conocida como prescripción no autorizada.
Asimismo, se dio a conocer que la FDA tomó esta decisión después de una solicitud de Gary Disbrow, director interino de la Autoridad de Investigación y Desarrollo Avanzado Biomédico.
El organismo había expresado previamente preocupaciones sobre el uso generalizado de hidroxicloroquina, emitiendo un aviso puntual a fines de abril que advertía contra el uso del medicamento fuera del entorno de un hospital o ensayo clínico.
CONTROVERSIA A NIVEL INTERNACIONAL
La controversia asociada al uso de la hidroxicloroquina no ha parado de crecer, en especial desde que dirigentes políticos como Donald Trump, Jair Bolsonaro o Nayib Bukele defendieran personalmente su uso terapéutico contra la COVID-19. La Casa Blanca incluso llegó a enviar dos millones de dosis de hidroxicloroquina a Brasil para combatir el coronavirus.
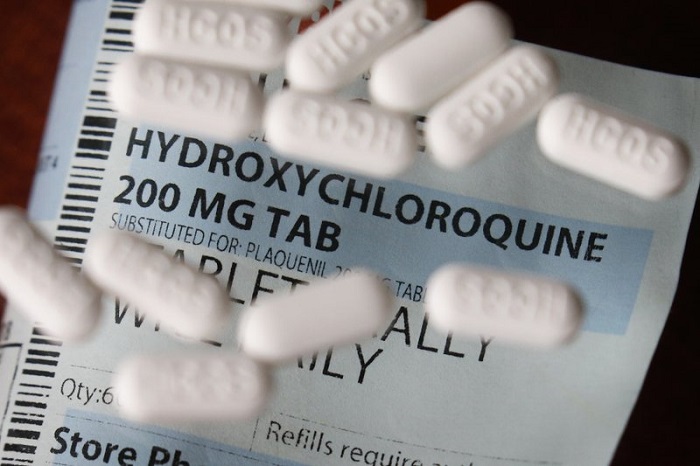
No obstante, el medicamento ha generado a nivel mundial dudas sobre si puede ser definido como tratamiento para el coronavirus, debido a la falta de evidencias sobre su efectividad, y algunas investigaciones han indicado que podría incluso perjudicar a los pacientes. Así, un estudio multinacional publicado en la revista The Lancet indicó que el fármaco reduce notablemente las posibilidades de supervivencia en pacientes con COVID-19.
Frente a esos hechos, la Organización Mundial de la Salud (OMS) anunció el pasado 25 de mayo la suspensión temporal de sus ensayos clínicos con hidroxicloroquina. No obstante, a principios de junio su director, Tedros Adhanom Ghebreyes, afirmó que la organización está dispuesta a reanudar las pruebas.
Entre tanto, y a la luz de esos mismos datos, el Gobierno francés tomó una decisión aún más determinante: suspender el uso de la hidroxicloroquina como fármaco contra la COVID-19 en su territorio.
Asimismo, los investigadores británicos decidieron el pasado 5 de junio poner fin a un masivo tratamiento experimental de pacientes diagnosticados con COVID-19 en el que se les administraba hidroxicloroquina. Los científicos explicaron que tomaron esta decisión luego de que los resultados iniciales no aportaran ninguna prueba de su efectividad clínica.
Por su parte, los investigadores de la Universidad de Minnesota (EU) determinaron el día anterior que el fármaco no es mejor que un placebo para prevenir la infección del coronavirus.
-Con información de Matthew Perrone, de AP

















































